1. Reaksi adisi
Reaksi-reaksi penting yang terjadi semuanya berpusat di sekitar ikatan rangkap. Biasanya, ikatan pi terputus dan elektron-elektron dari ikatan ini digunakan untuk menggabungkan dua atom karbon dengan yang lainnya. Alkena mengalami reaksi adisi.
Sebagai contoh, dengan menggunakan sebua molekul umum X-Y
Elektron-elektron yang agak terekspos dalam ikatan pi akan terbuka bagi serangan sesuatu yang membawa muatan positif. Elektron ini disebut sebagai elektrofil.
Beberapa jenis reaksi adisi yaitu:
· Adisi hidrogen dan Halogen ( Hidrogenasi and Halogenasi )
Ikatan pi dari alkena akan terpecah dari masing-masing pasangan elektonnya akan membentuk ikatan sigma yang baru ( atom karbon sp2 akan terhibridisasi membentuk atom karbon sp3 ).
Hidrogenasi alkena dengna katalis akan menghasilkan alakana
Reaksi Hidrogenasi adalah sebagai berikut:
Halogenasi alkena akan menghasilkann dihaloalkana
Reaksi Halogenasi adalah sebagai berikut:
X
Penambahan brom pada senyawa berikatan rangkap dilakukan sebgai salah satu identifikasi adanya ikatan rangkap. Reaksi dilakukan dengan menggunakan larutan bromin pada CCl4. Adanya ikatan rangkap ditujukkan dengan hilangnya warna coklat dari brom.
Proses reaksinya adalah sebagai berikut:
CH3CH = CHCH3 + Br2 → CH3CH CHCH3 2,3-dibromobutena
2-butena coklat Br (tidak berwarna)
· Adisi Halida Hidrogen (Hidrohalegenasi)
Hidrogen halida akan ditambahkan pada ikatan pi alkena membentuk alkil halida. Reaksi ini merupakan adisi elektrofilik.
Reaksi Adisi Halida Hidrogen adalah sebagai berikut:
CH2 = CH2 + HX → CH3CH2X
Etilena etil halida
Jika suatu alkena adalah alken asimetris (gugus terikat pada dua karbon sp3 yang berbeda), maka kemungkinan akan terbentuk 2 produk yang berbeda dengan adanya adisi HX.
CH3CH ≠ CHCH3 CH3CH ≠ CH2
Alkena simetris Alkens asimetris
Alkena simetris : CH3CH = CHCH3
CH3CH CHCH3
2-butena 2-klorobutena
Alkena asimetris :
Markonikov mengemukakan suatu teori untuk mengetahui pada rantai karbon yang mana atom H akan terikat. Menurut Markonikov, dalam adisi HX pada alkena asimetris, H+ dari HX akan menyerang ikatan rangkap karbon yang mempunyai jumlah atom H terbanyak. Dengan aturan Markonikov tersebut, maka produk yang akan terbentuk dapat diprediksi, seperti pada contoh berikut ini
2-kloropropana
Cl
Adisi asam halogen dapat mengikuti aturan Markonikov apabila berada dalam kondisi tanpa adanya peroksida dan berlangsung.
· Hidrobrominasi Alkena
Adisi hidrogen halida menggunakan HBr dan adanya peroksida (ROOR) disebut hidrobrominasi dan adisi yang terjadi adalah adisi anti Markonikov. Hal ini disebabkan oleh terbentuknya radiakl Br+ dari HBr. Ion Br+ ini akan menyerang ikatan rangkap atom karbon yang mempunyai jumlah atom H terbanyak dan membentuk radikal bebas yang stabil.
Reaksi hidrobrominasi adalah sebagai berikut: Br
Mekanisme reaksinya adalah sebagai berikut:
2. R−O + H−Br → R−O−H + Br
3. CH3CH = CH2 + Br → CH3 CH CH2
Br
4. CH3 CH CH2 + HBr → CH3 CH2 CH2 + Br+
Br Br
· Adisi H2SO4 dan H2O
Adisi asam sulfat pada alkena akan menghasilkan alkil hidrogen sulfat, yang selanjutnya akan digunakan dalam sintesis alkohol atau eter
CH3CH = CH2 + H−OSO3H → CH3CH − CH3
2-propil hidrogen sulfat
Pada larutan asam kuat (seperti larutan asam sulfat), air ditambahkan pada ikatan rangkap untuk menghasilkan alkohol. Reaksi ini disebut hidrosi alkena.
Propena 2-propanol (60%)
· Hidrasi menggunakan Merkuri asetat
Reaksi merkuri asetat Hg(O2CCH3)2 dan air pada alkena disebut oksimerkurasi. Produk oksimerkurasi biasanya direduksi dengan Natrium borohidrid (NaBH4), suatu rangkaian reaksi yang disebut demerkurasi. Reaksi ini terdiri dari 2 tahap reaksi yaitu adisi elektrofilik dari +HgO2OCH4 diikuti dengan serangan nukleofil H2O.
Proses reaksi Oksimerkurasi adalah sebagai berikut:
CH3CH2CH2CH = CH2
CH3CH2CH2CHCH2
1-pentena HgO2CCH3
Proses reaksi Demerkurasi adalah sebagai berikut:
CH3CH2CH2CHCH2− HgO2CCH3 CH3CH2CH2CHCH3 + Hg
· Adisi Boran
Diboran (B2H4) adalah gas beracun yang dibuat dari reaksi Natrium borohidrid dan Boron trifluorida (3 NaBH4 + 4 BF3 → B2H6 + 3 NaBF4). Pada larutan dietil eter, diboran terdisosiasi membentuk boran (BH3). Boran akan bereaksi dengan alkena membentuk organoboran (R2B). Reaksi ini teridri dari 3 langka reaksi. Dalam masing-masing tahap, satu gugus alkil ditambahkan dalam boran sampai semua atom hidrogen telah digantikan oleh gugus alkil. Reaksi ini disebut hidroborasi.
Mekanisme reaksinya adalah sebagai berikut:
Tahap 1
CH2 = CH2 + B – H → CH3 − CH2
Tahap 2
CH2 = CH2 + CH3CH2BH2 → (CH3CH2)2BH
Tahap 3
CH2 = CH2 + (CH3CH2)2BH → (CH3CH2)2B Trietil boran
Organoboran selanjutnya akan dioksidasi menjadi alkohol dengan hidrogen peroksida dalam larutan basa.
2. Reaksi Oksidasi
Alkena dapat dioksidasi menjadi berbagai macam produk, tergantung dari pereaksi yang digunakan. Secara umum, reaksi ikatan, rangkap karbon – karbon bisa diklasifikasikan menjadi :
1. Oksidasi ikatan pi tanpa pemecahan ikatan sigma ( ikatan C – C )
Produk reaksi ini bisa berupa 1,2 diol atau epoksida, tergantung dari pereaksi yang digunakan. Secara umum, reaksi ikatan rangkap karbon-karbon bisa diklasifikasikan menjadi:
Reaksi alkena dengan asam peroksikarboksilat (RCO3H atau ArCO3H) berupa asam peroksibenzoat ( C6H5CO3H ) dan m – kloroperoksibenzena dalam pelarut CHCl3 atau CCl4 akan menghasilkan epoksida atau oksiran.
−CH═CH2 + −COOH → −CH–CH + −COH
Stirene Asam Pheniloksiran (95%) Asam
m-khloroperoksibenzoat (Stiren oksida) m-klorobenzoat
Apabila sikloalkana direaksikan dengan OsO atau larutan KMnO4 dingin akan menghasilkan 1,2 diol.
CH2 = C
CH2−CH2n
CH2−CH2 + MnO2
O O
Reaksi dengan permanganat dingin disebut Baeyer Test,yaitu reaksi untuk
mengetahui ada tidaknya ikatan rangkap.Adanya ikatan rangkap ditunjukkan dengan hlangnya warna ungu dari KMnO4 . Pereaksi yang umum digunakan untuk mengubah alkena menjadi 1,2 diol dengan yield yang tinggi adalah Osmonium tetraoksida diikuti dengan reduksi menggunakan pereaksi Na2SO3 atau NaHSO3.
OSO4 Na2SO3 + Os
Sikloheksana O O OH
Os O OH
O cis – 1,2 - siklopentanadiol
1. Oksidasi ikatan pi diikuti pemecahan ikatan sigma
Apabila oksidasi ikatan pi disertai dengan pemecahan ikatan sigma, maka akan dihasilkan keton, asam karboksilat, maupun aldehid.
Jika masing – masing karbon alkena tidak terikat dengan atom hidrogen maka oksidasi akan menghasilkan keton.
H3C CH3 H3C CH3
keton
Reksi kedua ozonolis adalah oksidasi atau reduksi dari ozonida. Jika ozonida mengalami reduksi, salah satu karbon tersubstitusi dari alkena akan memebentuk aldehid. Sebaliknya jika terjadi oksidasi, akan terbentuk asam karboksilat.
Oksidasi:
O O O O
C C H2O2 H+ CH3COH + CH3CCH3
H O CH3 asetaldehid aseton
Membentuk aldehid membentuk keton
Reduksi:
C C Zn CH3CH + CH3CCH3
H O CH3 H+, H2O asetaldehid aseton
Membentuk aldehid membentuk keton

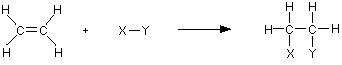













0 Komentar untuk "Reaksi- reaksi pada Alkena"
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)