RENCANA PELAKSANAAN PEMBELAJARAN
Prodi/Fakultas : Pendidikan Kimia Subsidi/MIPA
Nama Sekolah : SMK PIRI 1 YOGYAKARTA
Mata Pelajaran : Kimia
Kelas/Semester : X/I
Alokasi Waktu : 20 menit
Standar Kompetensi : 1. Mengidentifikasi struktur atom dan sistem periodik unsur
Kompetensi Dasar : 1.1 Memahami perkembangan struktur atom berdasarkan teori atom Dalton, Thomson, Rutherford, dan Bohr
1.2 Memahami sifat periodik unsur dalam tabel periodik unsur, massa atom relatif, dan perkembangan tabel periodik unsur
Indikator : 1.1.1 Menjelaskan sifat-sifat sinar katoda
1.1.2 Menjelaskan eksperimen yang dilakukan oleh J.J Thomson mengenai sinar katoda
1.1.3 Mendeskripsikan model atom J.J Thomson berdasarkan eksperimen sinar katoda
1.1.4 Menjelaskan kelebihan dan kelemahan model atom Thomson
I. Tujuan Pembelajaran
Siswa dapat :
1. Menjelaskan sifat-sifat sinar katoda
2. Menjelaskan eksperimen yang dilakukan oleh J.J Thomson mengenai sinar katoda
3. Mendeskripsikan model atom J.J Thomson berdasarkan eksperimen sinar katoda
4. Menjelaskan kelebihan dan kelemahan model atom Thomson
II. Materi Pembelajaran
1. Sifat-sifat sinar katoda
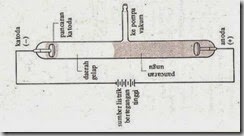
Gambar 1. Tabung Sinar Katoda
a) Sinar katoda dipancarkan oleh katoda dalam sebuah tabung hampa bila dilewati arus listrik (aliran listrik adalah penting)
b) Sinar katoda berjalan dalam garis lurus
c) Sinar tersebut bila membentur gelas atau benda tertentu lainnya akan menyebabkan terjadinya fluoresensi (mengeluarkan cahaya). Dari fluoresensi inilah kita bisa melihat sinar, sinar katoda sendiri tidak tampak.
d) Sinar katoda dibelokkan oleh medan listrik dan magnit; sehubungan dengan hal itu diperkirakan partikelnya bermuatan negatif
e) Sifat-sifat dari sinar katoda tidak tergantung dari bahan elektrodanya (besi, platina dsb.)
2. Eksperimen J.J Thomson
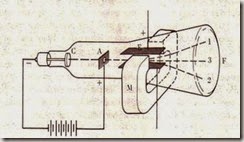
Gambar 2. Pengamatan Sinar Katoda yang dilakukan oleh J.J Thomson
Kode C = Katoda; A = Anoda; E = lempeng kondensor bermuatan listrik; M = magnet; F = layar berfluoresensi.
Berkas 1 : Hanya dengan adanya medan listrik, berkas sinar katoda dibelokkan keatas menyentuh layar pada titik 1.
Berkas 2 : Hanya dengan adanya medan magnit, berkas sinar katoda dibelokkan kebawah menyentuh layar pada titik 2.
Berkas 3 : Berkas sinar katoda akan lurus dan menyentuh layar dititik 3, bila medan listrik dan medan magnit sama besarnya
3. Model atom J.J Thomson
Berdasarkan eksperimen yang dilakukan oleh J.J Thomson, diperoleh kesimpulan sebagai berikut :
a) Kecepatan sinar katoda jauh lebih kecil dibandingkan kecepatan cahaya.
b) Perbandingan muatan listrik (e) dengan massa (m), e/m sinar katoda kira-kira 2 x 108 Coulomb per gram. Nilai ini sekitar 2000 kali lebih besar dari e/m yang dihitung dari hidrogen yang dilepas dari elektrolisis air (Thomson menganggap sinar katoda mempunyai muatan listrik yang sama seperti atom hidrogen dalam elektrolisis air).
c) Partikel sinar katoda bermuatan negatif dan merupakan partikel dasar suatu benda yang harus ada pada setiap atom. Pada tahun 1874 Stoney mengusulkan istilah elektron.
Model atom Thomson dikenal dengan model plum pudding/roti kismis.
Gambar 3. Model Atom J.J Thomson
4. Kelebihan model atom Thomson :
Membuktikan adanya partikel lain yang bermuatan negatif dalam atom. Berarti atom bukan merupakan bagian terkecil dari suatu unsur.
Kelemahan model atom Thomson :
Model Thomson tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut
III. Metode Pembelajaran
1. Ceramah
2. Tanya jawab
3. Tugas
IV. Langkah-langkah Pembelajaran
A. Kegiatan Awal (alokasi waktu ± 5 menit)
1) Membuka Pelajaran
a. Salam, berdoa, presensi, dan mengecek kesiapan siswa
b. Menyampaikan tujuan pembelajaran
2) Apersepsi
a. Menanyakan kepada siswa mengenai atom itu apa?
b. Mengingatkan kembali materi pelajaran teori atom Dalton mengenai model atom Dalton dan kelemahan dari model atom Dalton.
3) Masalah
Menyampaikan topik dan masalah yang akan dibahas :
Masalah : Apakah isi dari atom itu ?
Info : Salah satunya adalah elektron.
Topik : Penemuan elektron
B. Kegiatan Inti (alokasi waktu ± 12 menit)
1) Menjelaskan dan diskusi dengan siswa tentang sifat-sifat sinar katoda melalui penayangan ppt
2) Menjelaskan eksperimen penemuan elektron oleh J.J Thomson berdasarkan sinar katoda melalui penayangan ppt
3) Menyimpulkan sinar katoda = elektron
4) Membahas model atom Thomson setelah penemuan adanya elektron dalam atom
5) Menjelaskan kelebihan dan kelemahan model atom Thomson melalui penayangan ppt
6) Memberikan tugas kepada siswa mengenai materi teori atom J.J Thomson (terlampir)
C. Penutup (alokasi waktu ± 3 menit)
1) Evaluasi Proses
| No | Aspek | Skor (1-4) |
| 1 | Kehadiran mengikuti pelajaran | |
| 2 | Perhatian selama mengikuti pelajaran | |
| 3 | Keberanian menyatakan pendapat | |
| 4 | Keberanian bertanya | |
2) Rangkuman
J.J Thomson dapat menemukan elektron dan mengemukakan bahwa atom barada dalam keadaan stabil di alam dan memiliki muatan yang netral. Sehingga Thomson berasumsi didalam atom terdapat muatan positif. Model atom Thomson disebut juga plum pudding, atau dalam bahasa Indonesia dikenal dengan istilah roti kismis.
3) Memberikan pesan untuk pertemuan yang akan datang
V. Alat/Bahan/Sumber Bahan
A. Alat
1) LCD dan laptop
2) Papan tulis dan spidol
B. Bahan
1) Slide power point
C. Sumber bahan
Agustina Dwi Rahayu. (2011). Kupas Tuntas 1001 Soal Kimia. Jakarta: PT Buku Seru.
http://www.e-dukasi.net/index.php
Michael Purba. (2010). Kimia Untuk SMK. Jakarta: Erlangga.
VI. Penilaian
A. Teknik Penilaian : Tes tertulis (tugas rumah)
B. Bentuk Instrumen : Uraian
1) Soal
1. Sebutkan sifat-sifat sinar katoda !
2. Jelaskan bagaimana eksperimen yang dilakukan oleh J.J Thomson mengenai sinar katoda !
3. Jelaskan dan gambarkan model atom J.J Thomson berdasarkan eksperimen sinar katoda !
4. Sebutkan kelebihan dan kelemahan model atom Thomson !
2) Kunci jawaban
1. Sifat-sifat sinar katoda :
a) Sinar katoda dipancarkan oleh katoda dalam sebuah tabung hampa bila dilewati arus listrik (aliran listrik adalah penting)
b) Sinar katoda berjalan dalam garis lurus
c) Sinar tersebut bila membentur gelas atau benda tertentu lainnya akan menyebabkan terjadinya fluoresensi (mengeluarkan cahaya). Dari fluoresensi inilah kita bisa melihat sinar, sinar katoda sendiri tidak tampak.
d) Sinar katoda dibelokkan oleh medan listrik dan magnit; sehubungan dengan hal itu diperkirakan partikelnya bermuatan negatif
e) Sifat-sifat dari sinar katoda tidak tergantung dari bahan elektrodanya (besi, platina dsb.)
2. Eksperimen yang dilakukan oleh J.J Thomson dengan menggunakan sinar katoda digambarkan sebagai berikut :
Berkas 1 : Hanya dengan adanya medan listrik, berkas sinar katoda dibelokkan keatas menyentuh layar pada titik 1.
Berkas 2 : Hanya dengan adanya medan magnit, berkas sinar katoda dibelokkan kebawah menyentuh layar pada titik 2.
Berkas 3 : Berkas sinar katoda akan lurus dan menyentuh layar dititik 3, bila medan listrik dan medan magnit sama besarnya
Disimpulkan : Partikel sinar katoda bermuatan negatif dan merupakan partikel dasar suatu benda yang harus ada pada setiap atom. Pada tahun 1874 Stoney mengusulkan istilah elektron.
3. J.J Thomson menemukan elektron dan mengemukakan bahwa atom barada dalam keadaan stabil di alam dan memiliki muatan yang netral. Sehingga Thomson berasumsi didalam atom terdapat muatan positif. Model atom Thomson disebut juga plum pudding, atau dalam bahasa Indonesia dikenal dengan istilah roti kismis.
4. Kelebihan model atom Thomson : Membuktikan adanya partikel lain yang bermuatan negatif dalam atom. Berarti atom bukan merupakan bagian terkecil dari suatu unsur.
Kelemahan model atom Thomson : Model Thomson tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut
3) Pedoman penskoran
| No Soal | Skor |
| 1 | 25 |
| 2 | 25 |
| 3 | 25 |
| 4 | 25 |
| Jumlah | 100 |
Jumlah skor perolehan siswa x 100
Yogyakarta, 02 April 2012
Menyetujui





0 Komentar untuk "RPP Struktur Atom"
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)