1. Suatu atom X mempunyai konfigurasi elektron1s 22s 22p 63s 2. Senyawa dan yang dapat
dibentuk oleh atom ini adalah ........
A . HX2
B . XCl 2
C . CaX
D . X2(PO4) 3
E . X2SO4
Kunci : B
Penyelesaian :
Atom X termasuk golongan II A (alkali tanah)
Senyawanya dengan :
Ca tidak dapat membentuk senyawa
2. Di antara unsur-unsur 3P, 12Q, 19R, 33S dan 53T, yang terletak dalam golongan yang sama pada sistem periodik adalah ........
A . P dan Q
B . Q dan S
C . P dan R
D . S dan T
E . R dan T
Kunci : B
Penyelesaian :
3P 1s² 2s² (Golongan I A)
12Q 1s² 2s² 2p 6 3s² (Golongan II A)
19R 1s² 2s² 2p 6 3s² 3p 6 4s 1 (Golongan I A)
32S 1s² 2s² 2p 6 3s² 3p 6 4s² 3d 10 4p² (Golongan V A)
33T 1s² 2s² 2p 6 3s² 3p 6 4s² 3d 10 4p 6 5s² 4d 10 sp 5 (Golongan VII A)
3. Jika dalam volume 5 liter terdapat 4,0 mol asam yodida, 0,5 mol yod dan 0,5 mol hidrogen
dalam kesetimbangan pada suhu tertentu, maka tetapan kesetimbangan untuk reaksi
pembentukan asam yodida dari yod dan hidrogen adalah ........
A . 46
B . 50
C . 54
D . 60
E . 64
Kunci : E
Penyelesaian :
4. Untuk memperoleh konsentrasi Cl = 0,10 M, maka 250 mL, larutan CaCl 2= 0,15 M
harus diencerkan sampai .......
A . 500 mL
B . 750 mL
C . 1000 mL
D . 1250 mL
E . 1500 mL
Kunci : B
Penyelesaian :
5. Larutan jenuh X(OH) 2mempunyai pH = 9. Hasil kali larutan (Kp) dari X(OH) 2adalah
........
A . 10 -10
B . 5 x 10 -11
C . 10 -11
D . 5 x 10 -16
E . 10 -18
Kunci : D
Penyelesaian :
PH = 9 POH = 14 - 9 = 5
OH -= 10 -5
X(OH) 2 X +2+ 2OH
5 x 10 -4 . 10 -1
Ksp = [X 2+] [OH -]²
= (5 x 10 -4) (10 -5)² = 5 x 10 -16
6. Pada pembakaran 12 gram suatu persenyawaan karbon dihasilkan 22 gr gas CO2(A, C = 12, O = 16). Unsur karbon senyawa tersebut adalah .......
A . 23%
B . 27%
C . 50%
D . 55%
E . 77%
Kunci : C
Penyelesaian :
7. Volume larutan H2SO40,1 M yang diperlukan untuk mereaksikan 2,7 gram, logam Al (AR = 27) adalah .......
A . 1 L
B . 1,5 L
C . 3 L
D . 4,5 L
E . 5 L
Kunci : B
Penyelesaian :
8. Jika pada STP volume dari 4,25 gram gas sebesar 2,8 liter, maka massa molekul relatif
gas tersebut adalah .......
A . 26
B . 28
C . 30
D . 32
E . 34
Kunci : E
Penyelesaian :
9. Berapakah konsentrasi hidrogen fluorida dalam larutan HF 0,01 M yang terdisosiasi
sebanyak 20 % ........
A . 0,002 M
B . 0,008 M
C . 0,010 M
D . 0,012 M
E . 0,200 M
Kunci : B
Penyelesaian :
10. Untuk pembakaran sempurna 5 mol gas propana (C3H8), maka banyaknya mol gas
oksigen yang diperlukan adalah .......
A . 1
B . 3
C . 5
D . 15
E . 25
Kunci : E
Penyelesaian :
Reaksi pembakaran sempurna gas propana :
O2 yang diperlukan untuk 5 mol C3H8= 5 . 5 mol = 25 mol
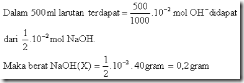
11. Larutan dengan pH = 12 dibuat dengan melarutkan larutan X gram NaOH (Mr = 40)
dalam air sampai 500 mL Besarnya X adalah ........
A . 4,0
B . 2,0
C . 1,0
D . 0,4
E . 0,2
Kunci : E
Penyelesaian :
Diketahui : pH larutan = 12
POH = 14 - 12 = 2 ..... [OH -] = 10 -2M
12. Banyaknya Fe -yang dapat dioksidasi oleh 1 mol menghasilkan Fe 3+dan Cr 3+ adalah ........
A . 1 mol
B . 2 mol
C . 3 mol
D . 4 mol
E . 6 mol
Kunci : E
Penyelesaian :
13. Jika konsentrasi Ca 2+ dalam larutan jenuh CaF 2 = 2 x 10-4 mol/L, maka hasil kali
kelarutan CaF2 adalah ......
A . 8 x 10 -8
B . 3,2 x 10 -11
C . 1,6 x 10 -11
D . 2 x 10 -12
E . 4 x 10 -12
Kunci : B
Penyelesaian :
CaF2 Ca 2+ + 2F -
Diketahui konsentrasi Ca 2+ = 2 . 10 -4 mol/L, maka :
konsentrasi F - = 2 x (2 . 10 -4) = 4 . 10 -4, jadi :
Ksp CaF2 = [Ca 2+] [F -] 2
= (2 x 10 -4) (4 x 10 -4)²
= (2 x 10 -4) (16 x 10 -8)
= 32 x 10 -12
= 3,2 x 10 -11
14. Sebanyak 92 gram senyawa karbon dibakar sempurna menghasilkan 132 gram karbon
dioksida (Mr = 44) dan 72 gram air (Mr = 18). Rumus empirik senyawa karbon tersebut
adalah ......
A . C2H2O2
B . C3H8O3
C . C4H10O2
D . C5H12O
E . C6H14
Kunci : B
Penyelesaian :
sehingga rumus empirik senyawa, menjadi C3H8O3
15. Pada suhu tertentu 0,350 gr BaF 2 (Mr = 175) melarut dalam air murni membentuk 1 L
larutan jenuh. Hasil kali kelarutan BaF 2 pada suhu itu adalah .......
A . 1,7 x 10 -2
B . 3,2 x 10 -6
C . 3,2 x 10 -8
D . 3,2 x 10 -9
E . 4,0 x 10 -9
Kunci : C
Penyelesaian :
16. Nomor atom Q = 20 dan nomor atom S = 8. Jika Q dan S membentuk senyawa QS,
maka senyawa ini memiliki ikatan ......
A . kovalen polar
B . kovalen non polar
C . kovalen koordinasi
D . ion
E . hidrogen
Kunci : D
Penyelesaian :
Konfigurasi elektron :
20Q = 1s² 2s² 2p 63s² 3p 6 4s² (golongan IIA)
8S = 1s² 2s² 2p 1(golongan VI A)
Ikatan yang mungkin terjadi antara Q (logam alkali tanah dan S (non logam) adalah ikatan
ion (serah terima elektron).
17. Dari beberapa unsur berikut yang mengandung :
1. 20 elektron dan 20 netron
2. 10 elektron dan 12 netron
3. 15 proton dan 16 netron
4. 20 netron dan 19 proton
5. 12 proton dan 12 netron
Yang memiliki sifat mirip dalam sistem periodik adalah ........
A . 1 dan 2
B . 2 dan 3
C . 2 dan 4
D . 3 dan 4
E . 1 dan 5
Jawaban : E
Penyelesaian :
1. 20 elektron dan 20 neutron
20X = 4 2 8 8 2 : Golongan IIA, Periode 4
2. 10 elektron dan 12 neutron
10X = 2 8 Golongan VIII A, Periode 2
3. 15 proton dan 16 neutron
15X = 2 8 5 : Golongan VA, Periode 3
4. 20 neutron dan 19 proton
19X = 4 2 8 8 1 : Golongan IA, Periode 4
5. 12 proton dan 12 neutron
12X = 2 8 2 : Golongan IIA, Periode 3
Unsur yang terletak di dalam satu satu golongan akan memiliki sisfat yang mirip jadi pilihan
yang tepat adalah 1 dan 5.
18. Tabung gas LPG mengandung gas propana (C 3H8) dan gas butana (C 4H10) di mana
sangat dipergunakan dalam kehidupan rumah tangga selain minyak tanah.
Jika campuran gas yang terdapat pada tabung pada gambar di atas volumenya 20 1iter
dibakar dengan udara yang mengandung 20% gas oksigen, maka udara yang diperlukan
sebanyak ........
A . 500 liter
B . 650 liter
C . 1000 liter
D . 1150 liter
E . 1300 liter
Jawaban : D
Penyelesaian :
(C 3H8 + C 4H10) + O2 7 CO 2 + 9 H 2O
20 liter
Udara mengandung 20% gas oksigen, maka :
Volume udara yang diperlukan = x 230 = 1150 liter.
19. Pada reaksi belum setara :
H2SO4 + HI H2S + I 2+ H2O
Satu mol asam sulfat dapat mengoksidasi hidrogen yodida sebanyak ......
A . 1 mol
B . 2 mol
C . 4 mol
D . 6 mol
E . 8 mol
Kunci : E
Penyelesaian :
Dengan menyetarakan reaksi didapat persamaan :
H2SO4 + HI H2S + I 2+ H2O
Jadi hidrogen yodida yang dapat dioksidasi = 8
20. Pupuk urea CO(NH2) 2mengandung nitrogen 42 %. Jika Mr urea = 60 dan A, N = 14,
maka kemurnian pupuk urea adalah ......
A . 45 %
B . 60 %
C . 75 %
D . 75 %
E . 98 %
Kunci : D
Penyelesaian :
Pupuk urea : CO(NH2) 2mengandung nitrogen 42 %
21. Pada suhu dan tekanan sama, 40 mL P 2 tepat habis bereaksi dengan 100 mL, Q2
menghasilkan 40 mL gas PxOy. Harga x dan y adalah .....
A . 1 dan 2
B . 1 dan 3
C . 1 dan 5
D . 2 dan 3
E . 2 dan 5
Kunci : E
Penyelesaian :
Persamaan reaksi yang terjadi :
xP 2+ yO2 2PxOy
volum 40 mL 100 mL 40 mL
karena perbandingan volume = perbandingan koefisien
22. Tetapan disosiasi suatu asam berbasa satu adalah 10 -7. Jika suatu larutan asam ini
mempunyai pH = 4 maka konsentrasinya adalah .......
A . 10 -1M
B . 10 -3M
C . 10 -4M
D . 10 -5M
E . 10 -7M
Kunci : A
Penyelesaian :
Untuk asam berbasa satu HA [H +] + [A]
pH = - log [H +]
4 = - log [H +]
[H +] = 10 -4mol/lt
23. Senyawa berikut yang mengandung jumlah molekul paling banyak adalah ......
A . 10,0 gr C2H6(Mr = 30)
B . 11,0 gr CO2(Mr = 44)
C . 12,0 gr NO2(Mr = 46)
D . 17,0 gr Cl 2(Mr = 71)
E . 20,0 gr C6H6(Mr = 78)
Kunci : A
Penyelesaian :
Mencari jumlah molekul terbanyak berarti mencari mol terbesar :
24. Jika diketahui massa atom relatif Fe = 56, S = 32 dan O = 16, maka massa besi yang
terdapat dalam 4g Fe 2(SO4) 3adalah .......
A . 4,00 g
B . 1,12 g
C . 0,01 g
D . 0,56 g
E . 0,28 g
Kunci : B
Penyelesaian :
Massa besi yang terdapat dalam 4 gram Fe 2(SO4) 3 adalah :
25. Bila pada suhu tertentu, kecepatan penguraian N2O5menjadi NO2dan O2adalah 2,5 x 10 -6 mol/L.s maka kecepatan pembentukan NO2adalah ....
A . 1,3 x 10 -6mol/L.s
B . 2,5 x 10 -6mol/L.s
C . 3,9 x 10 -6mol/L.s
D . 5,0 x 10 -6mol/L.s
E . 6,2 x 10 -6mol/L.s
Kunci : D
Penyelesaian :
Perhatikan reaksi berikut :
2N2O5 4NO2+ O2
Perbandingan kecepatan reaksi sesuai dengan perbandingan koefisien reaksi :
Jadi :



















1 Komentar untuk "Soal- Soal Kimia Stokiometri beserta Pembahasannya"
Assalamualaikum kakak..sayah mau soal nya yah..e-mail sayah yomanmyman51@gmail.com
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)