Pilihlah salah satu jawaban A,B,C,D atau E yang paling benar !
1. Bila ion Q mempunyai konfigurasi elektron (Ar)4s2 3d104p6 maka muatan ion tersebut adalah...
- + 6
- + 4
- + 2
- ─ 2
- ─ 4
2. Unsur P dan Q dapat membentuk molekul dan bentuk molekul ....
- PQ2 dan linier
- PQ2 dan bentuk V
- QP2 dan linier
- QP2 dan bentuk V
- P2Q5 dan trigonal bipyramida
3. Unsur Q terletak pada periode dan golongan....
- 3 dan IVA
- 3 dan IV B
- 4 dan IV A
- 4 dan VI A
- 4 dan VI B
4. Perhatikan data berikut:
| unsur | Sifar Unsur |
| A | § Dapat membentuk ion +1 § Molekulnya diatomik |
| B | § Molekulnya bersifat oksidator kuat § Pembentuk asam lemah |
Ikatan yang terjadi antar molekul A dan B adalah....
- ion
- kovalen
- hidrogen
- elektrovalen
- kovalen non polar
5. Perbandingan massa Belerang dan Oksigen dalam senyawa SO3 adalah 2 : 3. Untuk memperoleh 40 gram SO3, diperlukan belerang seberat....
- 16,0 gram
- 24,0 gram
- 26,7 gram
- 66,7 gram
- 100 gram
6. Udara mengandung 78% gas Nitrogen. Polusi udara dapat mengakibatkan kabut. Kabut terjadi karena ozon mudah mengoksidasi NO membentuk NO2 (warna coklat), dengan tahapan reaksi sebagai berikut:
On + O2 → O3
O3 + NO → NO2 + O2
Hasil reaksi pada tahap akhir adalah....
- Ozon
- Onascen
- Nitogen monoksida
- Nitrogen dioksida
- Dinitrogen oksida
7. Data hasil percobaan daya hantar listrik sebagai berikut :
| Larutan | Lampu | Gelembung Gas |
| A | Redup | Sedikit |
| B | Menyala Terang | Banyak |
| C | Redup | Banyak |
| D | Tidak Menyala | Sedikit |
Pernyataan yang benar tentang data tersebut adalah....
A. Daya hantar larutan A sama dengan larutan C
B. Daya hantar larutan B sama dengan larutan C
C. Daya hantar larutan A sama dengan larutan D
D. Larutan D non elektrolit
E. Larutan B elektrolit kuat
8. Untuk memperkirakan pH facial foam digunakan beberapa indikator, apabila ditetesi dengan metil jingga warna larutan menjadi kuning, ditetesi dengan metil merah warna larutan menjadi kuning dan dengan brom timol biru warna larutan menjadi hijau . Bila trayek perubahan warna dari indikator:
Metil Jingga (MJ) 3,1 – 4,4 Merah - Kuning
Metil Merah (MM) 4,2 – 6,3 Merah – Kuning.
Brom Timol Biru (BTB) 6,0 – 7,6 Kuning – Biru.
Maka perkiraan pH facial foam tersebut adalah...
- 3,1 - 4,2
- 4,2 – 4,4
- 4,4 – 6,0
- 6,0 – 6,3
- 6,3 – 7,6
9. Sebanyak 7,4 gram Ca(OH)2 ditimbang dan dilarutkan sampai volume 500 mL larutan, pH larutan adalah.... Ca= 40, O = 16 dan H = 1)
- 1 – log 2
- 1 – 2 log 2
- 13 – 2 log 2
- 13 + log 2
- 13 + 2 log 2
M = 7,4/74 x 1000/500 = 0,2 M
[OH-] = valensi x Mb = 2 x 0,2 M = 4 x 10-1
pOH = 1 – log 4
pH = 14- ( 1-log 4 ) = 13 + log 22 = 13 + 2 log 2
10. Larutan 10 mL Ba(OH)2 0,1 M ditetesi dengan indikator phenolphthalein, dititer dengan larutan HCl membutuhkan 9 mL sampai warna merah muda tepat hilang. Konsentrasi larutan HCl yang digunakan untuk pentiter adalah....
- 0,556 M
- 0,222 M
- 0,056 M
- 0,111 M
- 0,010 M
Pembahahasan no 11 s.20 sudah di page kimmuz.com
11. Percobaan yang menghasilkan campuran penyangga adalah....
- 1 dan 2
- 1 dan 3
- 2 dan 3
- 2 dan 5
- 4 dan 5
12. Dari ke lima percobaan diatas, larutan yang mempunyai pH sama adalah....
- 1 dan 2
- 1 dan 3
- 1 dan 4
- 2 dan 3
- 4 dan 5
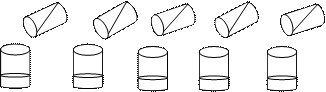
13. Ke dalam 5 buah gelas kimia masing-masing berisi 10 mL larutan dengan konsentrasi 0,001M ditambahkan 10 mL larutan 0,01M seperti terlihat pada gambar berikut!
NaBr NaCl Na2SO4 Na2CrO4 KSCN
AgNO3 Pb(NO3)2 AgNO3 BaCl2 AgNO3
I II III IV V
Dengan memperhatikan harga Ksp
AgBr 7,7 . 10-13
PbCl2 1,4 . 10-4
Ag2SO4 7,7 . 10 -5
BaCrO4 1,6. 10-10
AgSCN 1,0 . 10-12
Tabung reaksi yang terbentuk endapan adalah... .
- I dan II
- II dan III
- II dan IV
- III dan IV
- IV dan V
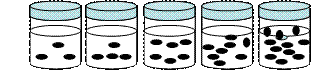
14. Perhatikan jumlah molekul yang terdapat dalam gelas kimia, volume zat pelarut sama
1 2 3 4 5
Larutan yang mempunyai kenaikan titik didih paling besar adalah....
- 1
- 2
- 3
- 4
- 5
15. Diagram PT pada fase H2O
T
S
E F G H Suhu
Yang merupakan daerah perubahan titik beku adalah ... .
A. A – S
B. T – C
C. B - F
D. E - F
E. G - H
16. Beberapa proses pembuatan koloid
1. agar-agar dalam air panas
2. larutan FeCl3 diteteskan ke dalam air mendidih
3. larutan AgNO3 diteteskan ke dalam larutan NaCl
4. Sol belerang dari belerang dan gula pasir
5. Minyak dicampur air dengan bantuan sabun
Pembuatan koloid dengan cara kondensasi adalah...
- 1 dan 2
- 1 dan 4
- 2 dan 3
- 3 dan 4
- 4 dan 5
17. Beberapa penerapan sifat koloid berikut:
1. proses pembentukan delta sungai
2. proses penjernihan air dengan tawas
3. penghamburan sinar sorotan lampu mobil
4. penyerapan racun oleh norit
5. cuci darah pada penderita ginjal
Yang merupakan sifat koagulasi dan efek Tyndall secara berurutan adalah ... .
- 1 dan 2
- 2 dan 3
- 2 dan 4
- 3 dan 4
- 4 dan 5
18. Jenis reaksi dari senyawa karbon diatas adalah...
- adisi
- oksidasi
- eliminasi
- substitusi
- kondensasi
19. Isomer fungsi dari hasil raeksi senyawa karbon diatas adalah...
- CH3 – CH2– CH2–O–CH2–CH3
- CH3 – CH2– CH2–CH2–O–CH3
- CH3 – CH2– CH2–CH2–OH
- CH3 – CH2– CHOH–CH2–CH3
- CH3 – CH2– CH2–CH2–COH
20. Kegunaan dari senyawa hasil reaksi diatas adalah....
A. pemanis
B. anaestesi
C. pengawet
D. antiseptik
E antioksidan
21. Senyawa karbon berikut yang tidak dapat dioksidasi adalah... .
- CH3-CHOH-CH3
- CH3-CH2- CH2OH
- (CH3-CH2)2CHOH
- CH3-CH2-CHOH-CH3
- (CH3)2COH-CH2-CH3
Jawab : E
Reaksi Oksidasi Alkohol sebagai berikut :
Alkohol Primer -- > Aldehid -- > Asam alkanoat
Alkohol Sekunder -- > keton
Alkohol tersier tidak dapat dioksidasi
OH
I
CH3 – C – CH2 – CH3
I
CH3
22. Jawab : A
22. Nama dari senyawa berikut :
Adalah …..
A. Benzaldehida
B. Benzyl alkohol
C. Asam benzoat
D. Fenil alkohol
E. Fenol
23. Perhatikan data polimer berikut :
| No | Polimer | Monomer | Terdapat Dalam… |
| 1. | Poli Etilena | Etena | Plastik |
| 2. | PVC | Vinil Klorida | Pipa Paralon |
| 3. | Poli Propilena | Propena | Tali Plastik, Botol Plastik |
| 4. | Teflon | Tetrafluoroetilena | Panci Anti Lengket |
| 5. | Poli Isopropen | Isopropena | Ban, Karet |
Dari data diatas, pasangan yang merupakan polimer alam adalah…
- 1
- 2
- 3
- 4
- 5
Jawab : E
Karet alam = poliisoprena
24. Beberapa ciri-ciri dari senyawa:
- mengandung gugus karboksil (COOH) dan gugus NH2 sehingga bersifat netral
- memiliki sifat hidrofobik (tidak larut dalam air) dan sifat hidrofilik (larut dalam air)
- pada suhu kamar berujud cair
- mempunyai titik didih yang berbeda berdasarkan kejenuhan ikatan
- merupakan polialkohol, mempunyai gugus aldehid atau keton
Ciri-ciri dari karbohidrat ditunjukkan oleh pernyataan nomor….
A. 1
B. 2
C. 3
D. 4
E. 5
Jawab : E
Pembahasan
1. Ciri asam amino
2. Ciri sabun yang mengandung gugus hidrofilik dan hidrofobik
3. Ciri lemak tak jenuh ( pada rantai karbonnya mengandung ikatan rangkap 2 )
4. Ciri lipida
5. Ciri dari glukosa, galaktosa
25. Tabung reaksi masing-masing diisi air dengan jumlah yang sama dan di ukur suhunya 27 oC, kemudian ke dalamnya dimasukkan zat berikut (perhatikan gambar) dan terjadi perubahan suhu.
Na2S2O3 (NH4)2SO4 KOH CO(NH2)2 Ba(OH)2
24 oC 25 oC 29 oC 26 oC 30 oC
Pernyataan yang benar proses pelarutan berdasarkan gambar tersebut adalah... .
A. Na2S2O3 bersifat endoterm karena mengambil panas
B. KOH bersifat eksoterm karena mengambil panas
C. (NH4)2SO4 bersifat eksoterm karena melepaskan panas
D. Ba(OH)2 bersifat endoterm karena mengambil panas
E. CO(NH2)2 bersifat endoterm karena melepaskan panas
Jawab : A
Pembahasan
Ciri reaksi eksoterm : terjadi kenaikan suhu
Ciri reaksi endoterm : terjadi penurunan suhu
26. Untuk menentukan perubahan entalpi pelarutan ammonium sulfat [(NH4)2SO4] ditimbang 6,6 gram zat tersebut dimasukkan ke dalam kalorimeter yang telah diisi dengan 100 mL air, setelah diaduk ternyata suhunya turun. Perhatikan gambar kalorimeter berikut!
Besarnya perubahan entalpi pelarutan ammonium sulfat adalah... .
( kalor jenis air = 4,2 jmol─K─ ; N=14, H=1, S=16, O=16)
Jawab : A
Mr = 132
m = massa zat = 100 gram ( massa terlarut diabaikan )
100 gram diambil dari massa air, karrena massa jenis air = 1 kg/L maka
100 mL air setara dengan 100 g
c = kalor jenis larutan
∆t = perubahan suhu, karena suhu turun maka reaksi bersifat endoterm (∆H =+ )
N = mol zat terlarut = massa/Mr = 6,6 / 132
27. Persamaan laju reaksi V=k[A]3[B] mempunyai harga tetapan laju reaksi 8.10 4 M-3 det -1
bila konsentrasi A dan B berturut-turut 0,02 M dan 0,125 M maka harga laju reaksi adalah...
A. 8. 1010 M/det
B. 8. 10-2 M/det
C. 8. 10-4 M/det
D. 1,25. 10-11 M/det
E. 1,25. 10-13 M/det
Jawab : B
V=k[A]3[B] = 8.10 4 [ 0,02 ]3 [0,125] = 8. 10-2 M/det
28. Direaksikan serbuk CaCO3 dengan 5 mL larutan HCl
CaCO3(s) + 2HCl(aq) à CaCl2(aq) + CO2(g) + H2O(l) Pada suhu 270C
| [HCl] | CaCO3 (mgram) | Waktu (det) |
| 1 M 1 M 1 M | 10 15 20 | 25 38 50 |
Faktor yang mempengaruhi laju terbentuknya gas CO2 adalah...
A. konsentrasi HCl
B. volume larutan
C. massa CaCO3
D. suhu
E. waktu
Jawab : C ( jelas )
29. Pembuatan NH3 dengan cara Haber-Bosch
N2(g)+ 3H2(g) « 2NH3(g) ∆H = ─ 92,38 kJ/mol dengan katalis besi pada suhu 550oC
Untuk mendapatkan gas NH3 yang lebih banyak maka dapat dilakukan...
A. Suhu dan tekanan dinaikkan
B. Suhu dan tekanan diturunkan
C. suhu diturunkan , tekanan diperbesar .
D. volum ruangan diperbesar, suhu dinaikkan
E. konsentrasi N2 diperbesar, suhu dinaikkan
Jawab : C
Mendapatkan NH3 lebih banyak berarti reaksi bergeser kea rah kana ( produk ), hal ini dapat dilakukan dengan cara :
- menurunkan suhu ( ke arah ∆H = ─ )
- memperbesar tekanan ( kea rah koefisien lebih kecil )
- memperkecil volume ( kea rah koefisien lebih kecil )
30. Dalam ruangan bervolume 5 liter terdapat 0,5 mol NH3, 1 mol N2 dan 0,5 mol H2 , dalam keadaan setimbang, dengan reaksi 2NH3(g) «N2(g)+3H2(g) harga tetapan kesetimbangan reaksi tersebut adalah...
Jawab : B ( jelas ),
[ mol/L ]
31. Pada reaksi Zn(s) + HNO3(aq) à Zn(NO3)2 (aq) + NH4 NO3(aq) + H2O(l)
Pernyataan yang benar menurut reaksi tersebut adalah... .
A. Zn sebagai oksidator dengan melepaskan 2 elektron
B. HNO3 sebagai oksidator dengan mengambil 8 elektron
C. HNO3 sebagai oksidator dengan mengambil 2 elektron
D. Zn(NO3)2 sebagai hasil reduksi
E. NH4 NO3 sebagai hasil oksidasi
Jawab : B
Zn (s) + HNO3(aq) à Zn(NO3)2 (aq) + NH4 NO3(aq) + H2O(l)
Biloks N = + 5 -3
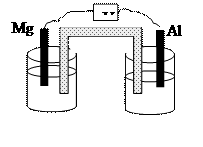
32. Perhatikan gambar sel volta berikut!
MgSO4 Al2(SO4)3(aq)
Al3+ + 3 e à Al E0 = – 1,66 V
Mg 2+ + 2 e à Mg E0 = – 2,37 V
Pernyataan yang benar tentang gambar tersebut adalah...
A. Elektroda Mg di katoda
B. Harga potensial sel + 4,03 V
C. Elektron mengalir dari elektroda Mg ke Al
D. Reaksi selnya Mg2+ / Mg// Al/ Al3+
E. Reaksi tidak dapat berjalan secara spontan
Jawab : C
E0 Mg = – 2,37 V < E0 Al = – 1,66 V, maka
Oksidasi Reduksi
Anoda Katoda
Reaksi sel : Mg/ Mg2+ // Al3+/ Al
Elektron mengalir dari anoda ke katoda
Perhatikan gambar berikut untuk mengerjakan soal nomor 33 dan 34
( I ) ( II )
NaI(aq) CuCl2(aq)
33. Pernyataan yang benar sesuai gambar tersebut adalah… .
A. Katoda di sel 1 menghasilkan iodin
B. Anoda di sel II menghasilkan gas klor
C. Katoda di sel II menghasilkan gas hidogen
D. Anoda pada sel 1 menghasilkan gas oksigen
E. Anoda di sel II menghasilkan endapan tembaga
Jawab : B
Na I CuCl2
CuCl2 -- >Cu2+ +2 Cl-
Katoda : Cu2+ + 2 e à Cu
Anoda : 2 Cl- à Cl2(g) + 2 e
NaI -- > Na+ + I-
Katoda : 2 H2O + 2 e -- > 2 OH- + H2 (g)
Anoda : 2 I- à I2 (s) + 2 e
34. Dialirkan arus listrik melalui 2 jenis larutan dalam rangkaian seri, (sesuai gambar) tesebut:
Jika dalam sel II dihasilkan 1,28 gram tembaga, maka volume gas (pada STP) yang dihasilkan di sekitar katoda sel I adalah .... (Ar Cu = 64 g/mol)
A. 896,0 mL
B. 448,0 mL
C. 224,0 mL
D. 89,6 mL
E. 44,8 mL
Jawab : B
Pada rangkaian seri jumlah arus yang diberikan pada kedua sel adalah sama , atau jumlah mol electron yang terlibat juga sama.
Pada sel dua : Cu yang dihasilkan 1,28 gram = 1,28/64 mol = 0,02 mol
Katoda : Cu2+ + 2 e à Cu
Maka mol elektronnya = 2x mol Cu = 0,04 mol
Padas el pertama,, gas H2 dihasilkan di katoda
Katoda : 2 H2O + 2 e -- > 2 OH- + H2 (g)
Berdasarkan data mol electron di sel ke dua = 0,04 mol, maka di sel pertama juga
0,04 mol
Dan mol H2 = ½ x mol elektronnya = 0,02 mol
Volume H2 = 0,02 x 22,4 L = 0,448 L = 448 mL
35. 
Besi paling cepat berkarat adalah besi pada percobaan nomor … .
A. ( 1 )
B. ( 2 )
C. ( 3 )
D. ( 4 )
E. ( 5 )
36. Beberapa mineral berikut:
1. pyrolusit
2. hematit
3. manganit
4. pasir kwarsa
5. gips
mineral yang mengandung logam Mn adalah... .
A. 1 dan 2
B. 1 dan 3
C. 1 dan 4
D. 2 dan 4
E. 4 dan 5
37. Beberapa pernyataan berikut
1. terbentuk gas hidrogen
2. terbentuk NaOH
3. memerahkan kertas lakmus
4. reaksi sangat eksplosif
5. logam Na bersifat oksidator
pernyataan yang benar bila logam Natrium dimasukkan ke dalam air adalah...
A. 1 dan 2
B. 2 dan 3
C. 3 dan 4
D. 3 dan 5
E. 4 dan 5
38. Pada reaksi 11Na23 + 0n1→ 12Mg24 + x. Partikel X adalah...
A. sinar beta
B. positron. 1X0
C. protium
D. netron
E. proton
untuk soal nomor 39 dan 40, gunakan wacana berikut :
Pengolahan aluminium secara industri dilakukan dengan cara elektrolisis lelehan Al2O3 dalam kriolit cair dengan menggunakan elektroda grafit (karbon). Kriolit berfungsi menurunkan titik leleh Al2O3 dari 2000 0C menjadi 1000 0C melalui reaksi berikut:
Al2O3(l) → 2 Al3+ + 3 O2–
Katoda : 2 Al3+ + 6 e– → 2 Al (l)
Anoda : 3 O2– →3/2O2(g) + 6 e–
Reaksi sel : Al2O3(l) → 2 Al(l) +3/2O2(g)
39. Nama proses pembuatan/pengolahan aluminium tersebut adalah....
- Hall - Herault
- Tanur tinggi
- Deacon
- Frasch
- Dow
40. Kegunaan logam yang dihasilkan dari proses tersebut adalah ….
A. pipa paralon
B. kerangka mobil
C. pembungkus makanan
D. kerangka pesawat terbang
E. elektrolit pada batu baterai





1 Komentar untuk "Prediksi UN KIMIA SMA 2015 dan Kunci jawaban"
jawaban nomor 14 apa ya?
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)