1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53 T yang terletak pada golongan yang sama dalam sistem periodik unsur adalah ........
A. P dan Q
B. P dan R
C. S dan T
D. Q dan S
E. R dan T
2. Unsur B, N, F dan H masing-masing mempunyai elektron valensi 3, 5, 7 dan 1. Antara unsur-unsur ini dapat terbentuk senyawa BF3NH3. Ikatan apakah yang terdapat dalam senyawa tersebut ........
- heteropolar dan homopolar
- heteropolar dan kovalen koordinasi
- homopolar dan kovalen koordinasi
- heteropolar
- kovalen koordinasi
3. Nomor atom unsur X sama dengan 27. Jumlah elektron tidak berpasangan dalam ion X2+ adalah ........
A. 1
B. 2
C. 3
D. 5
E. 7
4. Pada reaksi :
a K2MnO4 + b HCl MnO2 + c KMnO4 + d KCl + e H2O
Besarnya harga a, b, c, d dan e berturut-turut adalah ........
- 3 - 4 - 2 - 4 – 2
- 2 - 4 - 2 - 3 – 2
- 3 - 2 - 4 - 2 – 4
- 1 - 4 - 2 - 3 – 2
- 3 - 2 - 2 - 4 - 2
5. Pada suhu dan tekanan tetap, 160 ml campuran gas metana dan propana dibakar sempurna dengan 500 ml gas oksigen, maka persen volume gas propana di dalam campuran semula adalah ........
- 37,5%
- 43,7%
- 56,5%
- 62,5%
- 75%
6. Ke dalam 500 ml larutan asam nitrat 0,2 M ditambahkan larutan Na2CO3 melalui reaksi (belum setara) :
HNO3(aq) + Na2CO3(aq) NaNO3(aq) + H2O(l)+ CO2(g)
Pada suhu dan tekanan sama, 0,5 liter gas NO memiliki massa 7,5 gram (Mr = 30), maka volume gas CO2 yang dihasilkan sebanyak ........
- 250 ml
- 200 ml
- 175 ml
- 150 ml
- 100 ml
7. Perhatikan gambar berikut ini !
Reaksi yang menghasilkan endapan terdapat pada tabung reaksi ........
- 1 dan 2
- 2 dan 4
- 3 dan 4
- 2 dan 3
- 4 dan 5
8. Suatu paduan logam (aliasi) yang terdiri dari 90% Al (Ar = 27) dan 10% Cu (Ar = 63,5) digunakan untuk menghasilkan gas H2 dengan cara mereaksikannya dengan asam klorida. Untuk menghasilkan 6,72 liter gas H2 (STP), maka dibutuhkan paduan logam sebanyak ........
- 21,6 gram
- 12 gram
- 6,7 gram
- 6 gram
- 5,4 gram
9. Konsentrasi ion H+ yang terdapat dalam campuran 50 ml larutan H2SO4 0,2 M dengan 50 ml larutan CH3COOH 0,4M (Ka CH3COOH = 10-5) adalah ........
- 0,1 M
- 0,2 M
- 0,3 M
- 0,4 M
- 0,5 M
10. Ke dalam 90 ml larutan NH4OH 0,1 M (Kb NH4OH = 10 - 5) dicampurkan dengan 15 ml larutan H2SO4H 0,1M. Maka pH larutan yang terjadi adalah ........
- 5 - log 2
- 5 - log 4
- 8 + log 5
- 9 + log 2
- 9 + log 4
11. Diketahui garam-garam :
1. (NH4)2SO4 4. FeCl3
2. (CH3COO)2Ca 5. Na2CO3
3. Ba (NO3)2
Pasangan garam yang larutannya dalam air dapat mengubah lakmus biru menjadi merah adalah ........
2 dan 5
1 dan 4
3 dan 4
4 dan 5
2 dan 3
12. Sebanyak 3,16 gram (CH3COO)2Ca, Mr = 158 dilarutkan dalam air hingga volumenya
5 liter. Jika KaCH3COOH = 2 x 10-5, pH larutannya adalah ........
13. Dalam 200 ml larutan terdapat 2 x 10-5 mol Mg(OH)2 jenuh, maka kelarutan Mg (OH)2 dalam larutan pH = 12 + log 2 adalah ........
- 1,0 x 10-2 M
- 0,5 x 10-3 M
- 1,0 x 10-8 M
- 2,0 x 10-8 M
- 4,0 x 10-8 M
14. Dari lima macam larutan berikut yang mempunyai titik beku terendah adalah ........
- CO(NH2)2 0,05 M
- NaCl 0,03 M
- BaCl2 0,03 M
- AlCl3 0,02 M
- Fe2(SO4)3 0,02 M
15. Sebanyak 13,68 gram sukrosa (Mr = 342) dilarutkan dalam air sampai volume larutan 100 ml pada suhu 27° C, jika diketahui R = 0,082 L atm mol-1K-1, tekanan osmotik larutan tersebut adalah ........
- 9,84 atm
- 6,15 atm
- 4,92 atm
- 0,98 atm
- 0,092 atm
16. Fase terdispersi dan medium pendispersi pada kabut adalah ........
- cair dalam gas
- gas dalam cair
- padat dalam padat
- cair dalam padat
- padat dalam gas
17. Nama yang tepat untuk senyawa berikut adalah ........
- 2,5 dimetil - 5 etil - 2 pentena
- 2 - metil - 5 etil - 2 heksena
- 2 etil - 5 metil - 2heksena
- 3,6 dimetil - 5 heptena
- 2,5 dimetil - 2 heptena
18. Untuk meningkatkan bilangan oktan pada bensin dapat ditambahkan cat aditif yang lebih aman dari TEL yaitu MTBE rumus kimia MTBE adalah
........
- (CH3)2CH2COCH3
- (CH3)3COCH3
- (C2H5)4Pb
- (C2H5)4Pb
- (CH3)3CO2CH3
19. Senyawa yang dapat bereaksi dengan pereaksi Fehling atau Tollens memiliki gugus fungsi........
- O –
- CO –
- COOH
- CHO
- COO -
20. Pasangan senyawa karbon di bawah ini yang merupakan isomer gugus fungsi adalah ........
- propanol dan propanal
- metil etanoat dan propanol
- etil-metil-eter dan metil etanoat
- etil-metil-keton dan propanon
- propanol dan metoksietana
21. Turunan benzena berikut yang disebut paranitrofenol adalah ........
22. Sebanyak X molekul alanin (Mr = 89) berpolimerisasi kondensasi membentuk senyawa polipeptida. Jika Mr polipeptida 870. Mr H2O = 18, maka nilai X adalah ........
- 10
- 12
- 14
- 15
- 18
23. 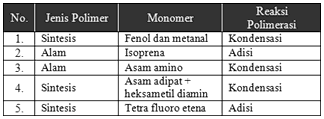
Berdasarkan data di atas, mana polimer yang sesuai dengan tabel no. 1 dan 4 adalah ........
- Bakelit dan Nilon
- Karet dan Protein
- Nilon dan Teflon
- Protein dan Nilon
- Polistirena dan Teflon
24. Dari beberapa karbohidrat berikut :
1. Fruktosa 4. Glukosa
2. Maltosa 5. Galaktosa
3. Laktosa
Karbohidrat yang dapat diserap oleh tubuh tanpa mengalami hidrolisis terlebih dahulu adalah ........
- 1, 2 dan 3
- 1, 3 dan 5
- 2, 3 dan 5
- 1, 4 dan 5
- 3, 4 dan 5
25. Data percobaan uji protein sebagai berikut:
Pasangan senyawa protein yang mengandung inti benzena adalah ........
- M dan N
- L dan N
- K dan L
- L dan M
- K dan M
26. Gas asetilena dapat dihasilkan dari reaksi :
CaC2(s) + 2H2O(l) Ca(OH)2(aq) + C2H2(g)
Kalor pembakaran gas asetilen 320 kJ/mol. Jika dalam suatu proses digunakan 320 gram Kalsium Karbida dengan asumsi hanya 60% CaC2 yang bereaksi, akan dihasilkan kalor sebanyak ........
- 320 kJ
- 480 kJ
- 640 kJ
- 800 kJ
- 960 kJ
27. H2O(l) H2(g) +
O2(g)
H = +68,3 kkal
H2(g) + O2(g)
H2O(g)
H = -57,8 kkal
H2O(l) H2O(s)
H = -1,4 kkal
Perubahan entalpi dari es menjadi uap adalah ........
- -11,9 kkal
- +11,9 kkal
- -91,0 kkal
- +9,1 kkal
- +12,47 kkal
28. Dalam suatu percobaan penentuan laju reaksi P + Q hasil, diperoleh data sebagai berikut:
Dari percobaan di atas dapat disimpulkan bahwa orde reaksi totalnya adalah ........
A. 1
B. 2
C. 3
D. 4
E. 5
29. Diketahui reaksi kesetimbangan pada suhu 725°C
4 NH3(g) + 5 O2(g) 4 NO(g) + 6 H2O(l)
H = -1169,5 kJ
Kesetimbangan dapat terganggu jika:
1. suhu dinaikkan 3. volume diperbesar
2. tekanan diperbesar 4. hasil reaksi dikeluarkan
Untuk memperoleh gas NO lebih banyak yang dapat dilakukan adalah ........
- 2 dan 4
- 2 dan 3
- 1 dan 4
- 1 dan 3
- 1 dan 2
30. Reaksi : 2 CO(g) + O2(g) 2 CO2(g)
Pada suhu tertentu 4 mol CO direaksikan dengan O2, ternyata dalam kesetimbangan terdapat 2 mol CO. Jika volume ruangan 10 liter dan harga tetapan kesetimbangan sama dengan 4, maka O2 yang diperlukan adalah ........
- 0,40 mol
- 0,25 mol
- 2,5 mol
- 3,5 mol
- 4 mol
31. Logam Fe (Ar Fe = 56) jika dilarutkan di dalam asam dan direaksikan dengan KMnO4 akan terjadi reaksi sebagai berikut:
Fe2+(aq) + Mn2+(aq) + Fe3+(aq)
Jika berat Fe yang dilarutkan 11,2 gram, maka volume KMnO4 0,1 M yang dibutuhkan untuk reaksi tersebut adalah ........
- 120 ml
- 160 ml
- 250 ml
- 320 ml
- 400 ml
32. Diketahui : E° dari :
Zn2+ | Zn = -0,76 V Cu2+ | Cu = +0,34 V
Fe2+ | Fe = -0,41 V Ag+ | Ag = +0,80 V
Pb2+ | Pb = -0,13 V
Sel kimia yang menghasilkan sel paling besar adalah ........
- Zn2+ | Zn || Cu2+ | Cu
- Fe2+ | Fe || Ag+ | Ag
- Zn2+ | Zn || Ag+ | Ag
- Pb2+ | Pb || Cu2+ | Cu
- Zn2+ | Zn || Pb2+ | Pb
33. Jika diketahui :
Zn + Cu2+ Zn2+ + Cu E° = +1,10 volt
Sn2+ + 2e Sn E° = -0,14 volt.
Cu2+ + 2e Cu E° = +0,34 volt.
Maka potensial standar bagi reaksi:
Zn + Sn2+ Zn2+ + Sn adalah ........
- +1,44 volt
- +0,62 volt
- +0,76 volt
- +0.96 volt
- +1,24 volt
34. Untuk menetralkan larutan yang terbentuk di Katode pada elektrolisis larutan Na2SO4 diperlukan 50 ml larutan HCl 0.2 M.
Jumlah muatan listrik yang digunakan adalah ........
- 0,01 F
- 0,02 F
- 0,05 F
- 0,10 F
- 0,20 F
Peristiwa elektrolisis dari ke empat gambar di atas yang menghasilkan gas hidrogen adalah........
- 1 dan 2
- 2 dan 3
- 1 dan 3
- 2 dan 4
- 3 dan 4
36. Diketahui potensial reduksi standar dari:
Al3+ | Al = -1,66 V Cu2+ | Cu = +0,34 V
Zn2+ | Zn = -0,76 V Ag+ | Ag = +0,80 V
Fe2+ | Fe = -0,44 V
Berdasarkan data tersebut, pasangan logam yang dapat mencegah terjadinya korosi pada Besi adalah ........
- Cu dan Zn
- Al dan Cu
- Cu dan Ag
- Zn dan Al
- Zn dan Ag
37. Di antara pernyataan berikut yang tidak tepat mengenai gas mulia adalah ........
- gas mulia merupakan golongan unsur yang bersifat inert.
- di alam gas mulia tidak bereaksi dengan unsur lain atau berada sebagai unsur bebas.
- di antara gas mulia hanya Xe yang dapat direaksikan dengan unsur lain pada kondisi tertentu
- bilangan oksidasi Xe dalam XeF6 dan dalam XeO3 adalah +6
- argon sebagai gas pengisi lampu penerang memiliki konfigurasi elektron terluar sebagai konfigurasi delapan.
38. Berdasarkan urutan sifat oksidator unsur-unsur halogen, maka reaksi redoks di bawah ini yang tidak mungkin berlangsung adalah ........
- Br2 + 2F-
F2 + 2 Br-
- Cl2 + 2Br-
2 Cl + Br2
- 2Br- + F2
2F- + Br2
- 2 I- + Br2
I2 + 2 Br
- 2 Cl- + F2
Cl2 + 2F
39. Pasangan garam alkali tanah yang menyebabkan kesadahan tetap pada air adalah ........
- CaSO4 dan Sr(HCO3)2
- CaCl2 dan MgCl2
- CaCl2 dan MgCl2
- Ca(HCO3)2 dan Mg (HCO3)2
- CaCl2 dan Ca(HCO3)2
40. Perhatikan tabel berikut:
Pasangan yang tepat antara senyawa dan kegunaannya adalah ........
- 1 dan b
- 2 dan a
- 4 dan c
- 2 dan d
- 2 dan d
41. Sifat di bawah ini yang sesuai untuk unsur-unsur periode ke tiga adalah ........
- Na paling sukar bereaksi
- P, S dan Cl cenderung membentuk basa
- S adalah logam
- Na, Mg, Al dapat berperan sebagai pengoksidasi
- energi ionisasi Ar paling besar
42. 16,25 gram logam unsur transisi yang bervalensi dua direaksikan dengan larutan HCl dan menghasilkan 5,6 dm³ gas hidrogen (STP). Jika atom ini mengandung 35 netron, maka konfigurasi logam tersebut adalah ........
- (Ar) 4s2 3d3
- (Ar) 4s2 3d5
- (Kr) 4s2 3d10
- (Ar) 4s2 3d10
- (Kr) 5s2 4d6
43. Manfaat elektrolisis dalam pembuatan tembaga adalah ........
- menaikkan kadar tembaga dalam bijihnya
- memisahkan bijihnya dari kotoran
- menghasilkan tembaga yang lebih murni
- menghilangkan kandungan peraknya
- membuat tembaga yang tahan karat
44. Dari suatu eksperimen dihasilkan gas X yang mempunyai sifat :
1. tidak berwarna
2. berbau menyengat
3. bila bereaksi dengan HCl pekat menghasilkan kabut putih
4. larutannya dapat mengubah lakmus merah menjadi biru.
Gas X tersebut adalah ........
- CO2
- NH3
- NO2
- SO2
- H2
45. Perhatikan gambar uji nyala dari ion alkali tanah berikut:
- 5 dan 2
- 1 dan 2
- 2 dan 5
- 1 dan 4
- 3 dan 5











0 Komentar untuk "Soal UN KIMIA Kelas XII bag.8"
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)