1. Persamaan reaksi berikut yang menunjukkan definisi perubahan entalpi pembentukan karbon monoksida adalah … .
2. Pada proses endoterm … .
A. kalor berpindah dari sistem ke lingkungan dan DH<0
B. kalor berpindah dari sistem ke ingkungan dan DH>0
C. kalor berpindah dari lingkungan ke sistem dan DH<0
D. kalor berpindah dari lingkungan ke sistem dan DH>0
E. tidak terjadi perpindahan kalor dan DH=0
3. Diketahui :
2C(grafit) + O2(g) 2CO(g) DH = - a kj/mol
C(grafit) + O2 CO2(g) DH = - b kj/mol
maka DH untuk reaksi CO(g) + O2(g)
CO2(g)
adalah … .
A. (-a – b) kj/mol
B. (a – b) kj/mol
E. (a + 2b) kj/mol
4. Dari diagram berikut :
maka harga DHf SnCl2(s) adalah … .
A. – 349,8 kJ/mol
B. +349,8 kJ/mol
C. +195,4 kJ/mol
D. -174,9 kJ/mol
E. +174,9 kJ/mol
5. Diketahui
N2(g) + 3H2(g) 2NH3(g) DH= - 107 kJ/mol
jika energi ikatan :
H – H : 436 kJ/mol
maka energi ikatan rata-rata N-H dalam NH3 adalah … .
A. 393 kJ/mol
B. 642 kJ/mol
C. 782 kJ/mol
D. 2249 kJ/mol
E. 2346 kJ/mol
laju reaksinya dapat dinyatakan sebagai … .
A. penambahan konsentrasi P tiap satuan waktu
B. penambahan konsentrasi Q tiap satuan waktu
C. pengurangan konsentrasi P dan Q tiap satuan waktu
D. pengurangan konsentrasi R tiap satuan waktu
E. pengurangan konsentrasi S tiap satuan waktu
7. Pada saat tercapai kesetimbangan dalam reaksi kimia, pernyataan berikut yang benar adalah … .
A. reaksi telah terhenti
B. mol pereaksi yang berubah sama dengan mol zat yang terbentuk
C. konsentrasi zat-zat campuran reaksi tidak berubah
D. laju reaksi ke kanan lebih cepat daripada laju reaksi balik
E. mol zat pereaksi sama dengan mol hasil reaksi
8. Data percobaan untuk reaksi: 2A + B2 2AB tersebut adalah sebagai berikut :
| No | [A] mol/lt | [B] mol/lt | Laju (mol/lt dt) |
| 1 2 3 | 0,5 1,0 1,0 | 0,5 0,5 1,0 | 1,5 x 10-2 3,0 x 10-2 3,0 x 10-2 |
Persamaan laju reaksinya adalah … .
A. v = k (A)2 (B2)
B. v = k (A) (B2)
C. v = k (B2)
D. v = k (A)0,5 (B2)
E. v = k (A)
9. Reaksi: NO(g) + Cl2(g) NOCl memiliki data :
| No | [NO] mol/lt | [Cl2(g)] mol/lt | Laju (mol/lt dt) |
| 1 2 3 | 0,5 0,5 0,15 | 0,5 0,15 0,05 | 1 x 10-3 3 x 10-3 9 x 10-3 |
maka orde reaksinya adalah … .
A. 0
B. 1
C. 2
D. 3
E. 4
10. Setiap kenaikan suhu 100C laju reaksi menjadi 2 kali lebih cepat dari semula. Jika pada suhu 200 C reaksi berlangsung selama 12 menit, maka laju reaksi pada suhu 500C adalah … .
A. 1,0 menit
B. 1,5 menit
C. 2,0 menit
D. 3,0 menit
E. 4,0 menit
11. Dalam suatu bejana 1 liter 4 mol gas NO2 membentuk kesetimbangan sebagai berikut :
dalam keadaan setimbang pada suhu tetap, masih terdapat NO2 sebanyak 1 mol, maka harga kc adalah … .
A. 2,7
B. 4,1
C. 6,75
D. 9,0
E. 13,5
12. Diketahui beberapa reaksi kesetimbangan sebagai berikut :
Reaksi kesetimbangan yang mempunyai harga tetapan kesetimbangan Kc = Kp adalah … .
A. 1 dan 2
B. 1 dan 3
C. 2 dan 3
D. 3 dan 4
E. 4 dan 5
13. Pada suhu 250C dan tekanan total 0,30 atm, tekanan parsial N2O4 adalah 0,15 atm, maka pada sistem kesetimbangan
Harga Kp adalah … .
C. 3,0 atm-1
14. Diketahui reaksi:
Spesi yang bersifat amfiprotik adalah ... .
A. H2S
B. H2O
C. H3O+
D. HS–
E. S2–
15. Dari reaksi:
Yang merupakan pasangan asam basa konyugasi adalah ... .
A. H2CO3 dan H2O
B. H2CO3 dan H3O+
C. H2CO3 dan HCO3–
D. H2O dan HCO3–
E. H3O+ dan HCO3–
16. Sistem kesetimbangan berikut tidak dipengaruhi oleh perubahan tekanan maupun volum.
D. 2Cl2(g) + 2H2O(g) 4HCl(g) + O2(g)
17. Campuran larutan HCl 0,1 M dengan larutan NH4OH 0,2 M [Kb = 1 x 10–5] mempunyai pH = 9, maka perbandingan volum HCl dengan volum NH4OH adalah ... .
A. 1 : 1
B. 1 : 2
C. 2 : 1
D. 2 : 3
E. 3 : 2
18. Untuk membuat larutan penyangga dengan pH = 5, maka ke dalam 50 ml larutan asam asetat 0,2 M (Ka = 1 x 10–5) harus ditambahkan larutan NaOH 0,5 M sebanyak ... .
A. 5 ml
B. 10 ml
C. 15 ml
D. 20 ml
E. 25 ml
19. Jika tetapan asam CH3COOH = 10–5, maka pH larutan CH3COONa 0,1 M adalah ... .
A. 5
B. 6
C. 8
D. 9
E. 10
20. Untuk menetralkan 25 ml larutan H2SO4 0,1 M diperlukan 20 ml larutan NaOH, maka konsentrasi larutan NaOH adalah ... .
A. 0,10 M
B. 0,15 M
C. 0,20 M
D. 0,25 M
E. 0,50 M

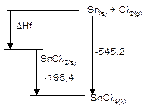

0 Komentar untuk "Soal (Ujian Nasional) Kimia Kelas XI bag.1"
Berkomentarlah dengan baik dan sopan, saya akan berusaha untuk menjawab setiap pertanyaan dan menanggapi setiap komentar yang anda berikan, :)
Terimakasih atas kunjungan dan komentarnya :)